صورة التصوير التبايني بالبقع الليزرية
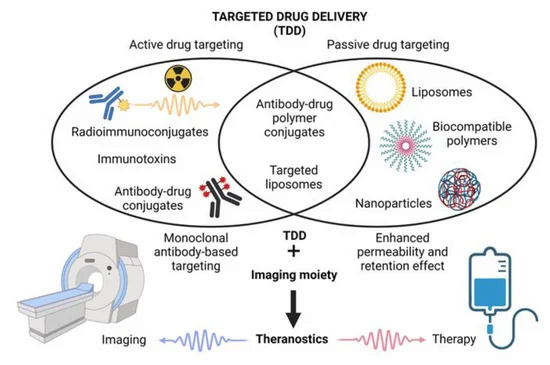
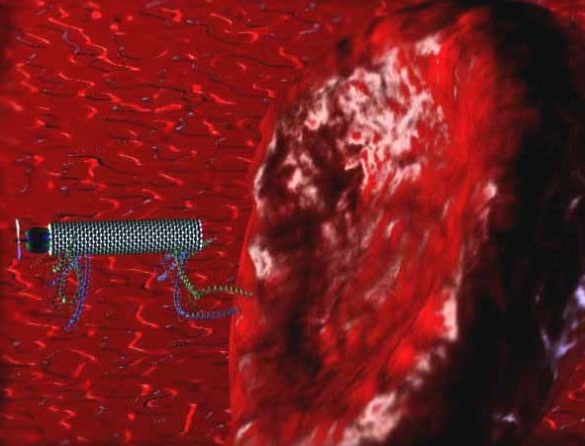
صورة توصيل الأدوية المستهدف داخل الأوعية الدموية
ما هي الروبوتات النانوية؟
Nanorobotics هو مجال التكنولوجيا الناشئ لإنشاء الآلات أو الروبوتات التي تكون مكوناتها على المقياس المجهري للنانومتر أو بالقرب منه. وبشكل أكثر تحديدًا، تشير الروبوتات النانوية إلى مجال هندسة تكنولوجيا النانو لتصميم وبناء الروبوتات النانوية، بأجهزة تتراوح في الحجم من 0.1 إلى 10 ميكرومتر ومصنوعة من مكونات نانوية أو جزيئية. تم أيضًا استخدام أسماء الروبوتات النانوية أو النانوية أو النانوية أو الآلات النانوية أو النانوميتية لوصف هذه الأجهزة قيد البحث والتطوير حاليًا.
بحلول عام 2020، يعتقد العلماء في جامعة روتجرز أنه سيتم حقن الروبوتات النانوية في مجرى الدم وإعطاء الدواء مباشرة إلى الخلية المصابة. يحتوي هذا الروبوت النانوي على جسم من أنابيب الكربون النانوية، وهو محرك جزيئي حيوي يدفعه وأطرافه الببتيدية لتوجيه نفسه. نظرًا لأنه يتكون من عناصر بيولوجية مثل الحمض النووي والبروتينات، فسيتم إزالته بسهولة من الجسم. (الصورة مقدمة من فريق Bio-Nano Robotics في جامعة روتجرز: كونستانتينوس مافروديس، مارتن إل. يارموش، أتول دوبي، أنجيلا ثورنتون، كيفن نيكيتشوك، وسيلفينا توماسوني، وفوتيوس باباديميتراكوبولوس، وبيرني يورك.)
الروبوتات النانوية هي أجهزة مجهرية نظرية تقاس بمقياس النانومتر (1 نانومتر يساوي جزءًا من المليون من 1 ملليمتر). وعندما يتم تحقيقها بالكامل من المرحلة الافتراضية، فإنها ستعمل على المستوى الذري والجزيئي والخلوي لأداء المهام في كل من المجالات الطبية والصناعية التي كانت حتى الآن مادة من الخيال العلمي.
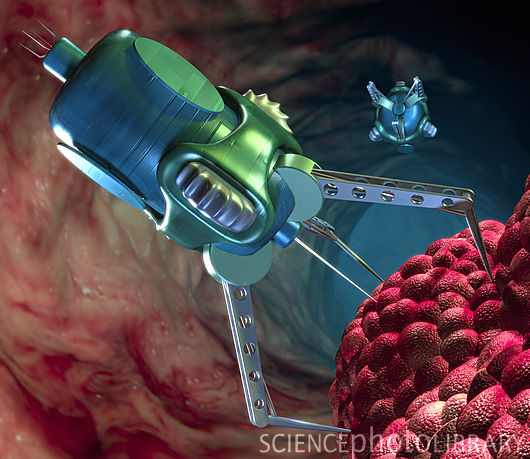
بعد بضعة أجيال من الآن قد يُعرض على شخص مصاب بالسرطان بديل جديد للعلاج الكيميائي، وهو العلاج التقليدي بالإشعاع الذي لا يقتل الخلايا السرطانية فحسب، بل الخلايا البشرية السليمة أيضًا، مما يسبب تساقط الشعر والتعب والغثيان والاكتئاب ومجموعة من الأمراض. أعراض أخرى. يمكن للطبيب الذي يمارس الطب النانوي أن يقدم للمريض حقنة من نوع خاص من الروبوت النانوي الذي يبحث عن الخلايا السرطانية ويدمرها، ويبدد المرض من المصدر، ويترك الخلايا السليمة دون مساس. لا تزال الآلات النانوية في مرحلة البحث والتطوير إلى حد كبير، ولكن تم اختبار بعض الآلات الجزيئية البدائية.
الروبوتات النانوية هي أجهزة مجهرية نظرية تقاس بمقياس النانومتر
قد تكون التطبيقات المفيدة الأولى لآلات النانو في مجال التكنولوجيا الطبية، والتي يمكن استخدامها لتحديد الخلايا السرطانية وتدميرها. في الآونة الأخيرة، عرضت جامعة رايس سيارة مكونة من جزيء واحد تم تطويرها بواسطة عملية كيميائية وتضم كرات بوكي للعجلات. على الرغم من أن عمليات تكنولوجيا النانو تحدث على نطاق النانومتر، إلا أن المواد والأشياء التي تنتج عن هذه العمليات يمكن أن تكون أكبر من ذلك بكثير. تحدث النتائج واسعة النطاق عندما تتضمن تقنية النانو توازيًا هائلاً حيث تتحد العديد من العمليات النانوية المتزامنة والتآزرية لإنتاج نتيجة واسعة النطاق.
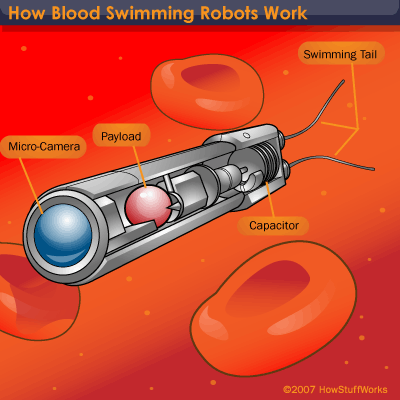
تمتد تقنية النانو وتدمج التخصصات التي تتعامل مع المادة على المستوى الجزئي (الفيزياء والكيمياء والأحياء) مع تلك التي تتعامل مع المادة على المستوى الكلي (الهندسة وعلوم المواد وعلوم الكمبيوتر). الروبوت النانوي عبارة عن آلة صغيرة مصممة لأداء مهمة أو مهام محددة بشكل متكرر وبدقة بأبعاد نانوية، أي أبعاد بضعة نانومترات (نانومتر) أو أقل، حيث 1 نانومتر = 10-9 متر. تمتلك الروبوتات النانوية تطبيقات محتملة في تجميع وصيانة الأنظمة المتطورة. قد تعمل الروبوتات النانوية على المستوى الذري أو الجزيئي لبناء أجهزة أو آلات أو دوائر، وهي عملية تعرف باسم التصنيع الجزيئي.
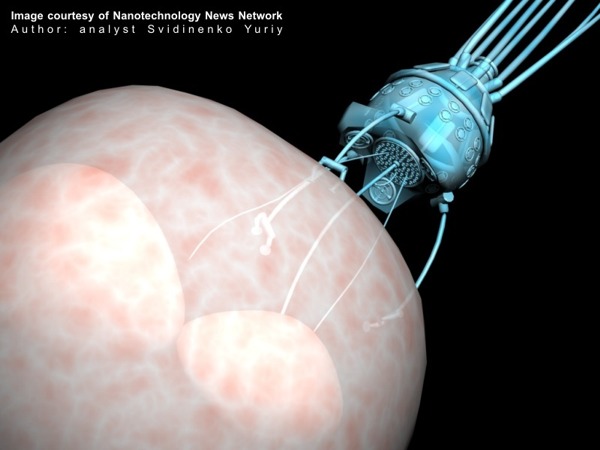
يقوم الروبوت النانوي بإجراء جراحة الخلايا
قد تنتج الروبوتات النانوية أيضًا نسخًا من نفسها لتحل محل الوحدات البالية، وهي عملية تسمى التكرار الذاتي. تحظى الروبوتات النانوية باهتمام خاص لدى الباحثين في الصناعة الطبية. يمكن للأنظمة النانوية أيضًا أن تعمل بشكل أسرع بكثير من نظيراتها الأكبر حجمًا لأن الإزاحات أصغر؛ وهذا يسمح بحدوث الأحداث الميكانيكية والكهربائية في وقت أقل وبسرعة معينة.
إن المعرفة الإنسانية، بكل نموها وتطورها، لا تزال في مراحلها الأولى من إيجاد طرق فعالة لعلاج السرطان. إن العدد المرتفع لمرضى السرطان يضع علاج السرطان ضمن الأولويات القصوى لمرافق البحث العلمي. إن ظهور تكنولوجيا النانو يفتح نوافذ جديدة تعد بطرق فعالة لتحديد المصادر الكيميائية وتتبعها والسيطرة على الخلايا السرطانية والقضاء عليها في النهاية.
الروبوت النانوي يهاجم السرطان
تتكاثر الخلايا السرطانية بشكل أسرع من الخلايا السليمة، مما يسبب إجهادًا في إمدادات العناصر الغذائية وفي التخلص من منتجات النفايات الأيضية. بسبب النمو السريع للخلايا السرطانية، لا تستطيع الخلايا السليمة التنافس للحصول على العناصر الغذائية الكافية، وسيتم استبدالها في النهاية بالخلايا السرطانية. في مرحلة ما، سيصل معدل نمو الورم إلى حالة مستقرة حيث يساوي معدل موت الخلايا معدل تكاثر الخلايا، ويبقى في حالة مستقرة حتى يتمكن الورم من الوصول بشكل أفضل إلى الدورة الدموية. العامل الحاسم في تحديد فرصة بقاء المريض على قيد الحياة هو مدى اكتشاف الخلايا السرطانية في وقت مبكر.
أحد الجوانب المهمة في علاج السرطان هو تطوير نظام توصيل الدواء المستهدف الذي يقلل من الآثار الجانبية السامة للعلاج الكيميائي. تتضمن الطريقة التقليدية الحالية في علاج السرطان إدخال القسطرة للسماح بالعلاج الكيميائي، لتقليل كمية السرطان الموجودة، ثم إزالة الأورام جراحيًا، يليها المزيد من جلسات العلاج الكيميائي والإشعاعي. تتنقل الروبوتات النانوية كأجهزة محمولة بالدم، بحيث يمكن استخدامها للمساعدة في تشخيص السرطان في مراحله المبكرة والمشاركة في توصيل الأدوية الذكية.
نظرًا لأن الروبوتات النانوية ستكون مجهرية الحجم، فمن المحتمل أن يكون من الضروري لأعداد كبيرة جدًا منها أن تعمل معًا لأداء المهام المجهرية والعيانية. يوفر الاستخدام المشترك للإلكترونيات النانوية والطباعة الحجرية الضوئية والمواد الحيوية الجديدة طريقة ممكنة لتصنيع الروبوتات النانوية للتطبيقات الطبية الشائعة، مثل الأجهزة الجراحية والتشخيص وتوصيل الأدوية. Nubots هي أجهزة روبوتية اصطناعية على مقياس النانو. تشمل الروبوتات النووية العديدة من سائري الحمض النووي التي أبلغت عنها مجموعة نادريان سيمان في جامعة نيويورك، ومجموعة نايلز بيرس في معهد كاليفورنيا للتكنولوجيا، ومجموعة جون ريف في جامعة ديوك، ومجموعة تشينغدي ماو في بوردو، ومجموعة أندرو توربرفيلد في جامعة أكسفورد.
تركز شركة Nanofactory Collaboration، التي أسسها روبرت فريتاس ورالف ميركل في عام 2000 وتضم 23 باحثًا من 10 منظمات و4 دول، على تطوير أجندة بحثية عملية تهدف تحديدًا إلى تطوير التخليق الميكانيكي للألماس الذي يتم التحكم فيه موضعيًا ومصنع النانو الماسي الذي سيكون لديه القدرة على البناء. الروبوتات النانوية الطبية الماسية. عادةً ما يتم تطبيق استخدام المجالات الكهرومغناطيسية للتحكم في حركة هذا النوع من الأجهزة البيولوجية المتكاملة.
تم توجيه وثيقة تحتوي على مقترح بشأن تطوير التكنولوجيا الحيوية النانوية باستخدام مناهج التكنولوجيا المفتوحة إلى الجمعية العامة للأمم المتحدة. بنفس الطريقة التي أدى بها تطور التكنولوجيا إلى سباق الفضاء وسباق التسلح النووي، يحدث سباق على الروبوتات النانوية. هناك أرضية واسعة تسمح بإدراج الروبوتات النانوية ضمن التقنيات الناشئة.
بعض الأسباب هي أن الشركات الكبيرة، مثل جنرال إلكتريك وهيوليت باكارد ونورثروب جرومان، عملت مؤخرًا على تطوير الروبوتات النانوية وأبحاثها، وبدأ الجراحون في المشاركة وبدأوا في اقتراح طرق لتطبيق الروبوتات النانوية في الإجراءات الطبية الشائعة والجامعات. ومعاهد البحوث تم منح أموال من قبل الوكالات الحكومية تتجاوز 2 مليار دولار أمريكي لأبحاث تطوير الأجهزة النانوية للطب، ويستثمر المصرفيون أيضًا بشكل استراتيجي بهدف الحصول مسبقًا على الحقوق والعائدات المتعلقة بتسويق الروبوتات النانوية في المستقبل. تم مؤخرًا منح عدد كبير من براءات الاختراع للروبوتات النانوية، معظمها لوكلاء براءات الاختراع، والشركات المتخصصة فقط في بناء محفظة براءات الاختراع، والمحامين.
ملخص البحث: تتبع وتوجيه أسراب الروبوتات النانوية المغناطيسية داخل الأوعية الدموية
الهدف:
- تتبع سرب من الروبوتات النانوية المغناطيسية داخل الأوعية الدموية في الوقت الفعلي.
- توجيه ملاحة سرب الروبوتات النانوية.
الطريقة:
- استخدام تقنية التصوير التبايني بالبقع الليزرية (LSCI).
النتائج:
- إمكانية التصوير عالي التباين والتنقل لسرب الروبوتات النانوية في بيئات الدم الراكدة والمتدفقة خارج الجسم الحي وفي الجسم الحي.
- تتبع سرب صغير من الروبوتات النانوية في الجسم الحي.
الخلاصة:
- توفر تقنية LSCI إمكانيات واعدة لتتبع وتوجيه أسراب الروبوتات النانوية في الأوعية الدموية.
- يمكن أن تُستخدم هذه التقنية لتحسين عملية التوصيل المستهدف داخل الأوعية الدموية.
النقاط الرئيسية:
- أسراب الروبوتات الدقيقة/النانوية لها إمكانات كبيرة في التطبيقات الطبية.
- تتبع أسراب الروبوتات الدقيقة/النانوية في الجسم الحي يمثل تحديًا.
- تقنية LSCI تسمح بتتبع وتوجيه أسراب الروبوتات النانوية في الوقت الفعلي.
- تتمتع تقنية LSCI بدقة زمنية ومكانية عالية، وعدم التدخل.
- يمكن استخدام تقنية LSCI لتحسين عملية التوصيل المستهدف داخل الأوعية الدموية.
المصطلحات:
- أسراب الروبوتات الدقيقة/النانوية: مجموعة من الروبوتات الصغيرة جدًا التي تعمل معًا.
- التصوير التبايني بالبقع الليزرية (LSCI): تقنية تصوير تسمح بتصوير الأجسام الصغيرة جدًا بدقة عالية.
- التوصيل المستهدف داخل الأوعية الدموية: توصيل الأدوية أو المواد الأخرى إلى موقع محدد داخل الجسم باستخدام الروبوتات الدقيقة/النانوية.
ملاحظات:
- هذا ملخص قصير للبحث، يرجى الرجوع إلى الورقة الأصلية لمزيد من التفاصيل.
- تم استخدام مصطلحات علمية محددة في هذا الملخص، يرجى الرجوع إلى مصادر علمية موثوقة لشرحها.
ملاحظة:
- يرجى استخدام محرك بحث Google للعثور على مصادر علمية موثوقة لشرح المصطلحات العلمية.
مفاهيم متقدمة:
- التحكم المغناطيسي: استخدام المجالات المغناطيسية للتحكم في حركة الروبوتات النانوية.
- التصوير بالرنين المغناطيسي (MRI): تقنية تصوير تسمح بتصور الأنسجة الداخلية للجسم.
- التوصيل الموجه: توصيل الأدوية أو المواد الأخرى إلى موقع محدد داخل الجسم باستخدام تقنيات متقدمة.
أمثلة على تطبيقات تقنية LSCI:
- توصيل الأدوية إلى الأورام السرطانية.
- إزالة الجلطات الدموية.
- علاج أمراض القلب.
- تحسين جراحة الدماغ.
مستقبل تقنية LSCI:
- تطوير تقنيات جديدة لتصنيع الروبوتات النانوية.
- تحسين دقة تقنية LSCI.
- توسيع نطاق تطبيقات تقنية LSCI.
أهمية البحث:
- يقدم هذا البحث تقنية جديدة واعدة لتتبع وتوجيه أسراب الروبوتات النانوية داخل الأوعية الدموية.
- يمكن أن تؤدي هذه التقنية إلى ثورة في مجال الطب من خلال تحسين توصيل الأدوية والعلاجات إلى مواقع محددة داخل الجسم.
- دورة "علم الأعصاب وفسيولوجيا الجهاز العصبي" من جامعة هارفارد:
مميزات الدورة:
- مقدمة شاملة لعلم الأعصاب وفسيولوجيا الجهاز العصبي.
- تشرح الدورة بنية ووظائف الجهاز العصبي المركزي والمحيطي.
- تناقش الدورة الأمراض العصبية الشائعة مثل الخرف ومرض باركنسون.
- تتضمن الدورة محاضرات ومواد تفاعلية واختبارات.
محتوى الدورة:
- الوحدة 1: مقدمة لعلم الأعصاب
- الوحدة 2: الخلايا العصبية والاتصال العصبي
- الوحدة 3: الجهاز العصبي المركزي
- الوحدة 4: الجهاز العصبي المحيطي
- الوحدة 5: الحواس
- الوحدة 6: الحركة
- الوحدة 7: التعلم والذاكرة
- الوحدة 8: الاضطرابات العصبية
متطلبات الدورة:
- لا توجد متطلبات مسبقة.
- يُنصح بوجود خلفية في علم الأحياء أو علم وظائف الأعضاء.
ملاحظة:
- هذه الدورة مجانية.
- تتوفر الدورة باللغة الإنجليزية فقط.
كتب
- Microrobotics by William H. Grover (2010)
- Nanorobotics by Bharat Bhushan (2010)
يفتح الرابط في نافذة جديدة.
link.springer.com
Book Nanorobotics by Bharat Bhushan- Introduction to Nanorobotics by Satoshi Tadokoro (2012)
كتب عن التصوير التبايني بالبقع الليزرية (LSCI):
- Laser Speckle Contrast Imaging by David J. D. Earnest (2017)
- Handbook of Biomedical Optics by David A. Boas and Joseph A. Izatt (2011)
كتب عن التوصيل المستهدف داخل الأوعية الدموية:
- Targeted Drug Delivery by Kenneth A. J. McEvoy (2005)
- Drug Delivery: Principles and Applications by V. V. Ranade and V. J. Kulkarni (2015)
القائمة المذكورة هي مجموعة شاملة من المراجع حول الروبوتات الدقيقة لتوصيل الأدوية المستهدفة. تتضمن مقالات من مختلف المجلات العلمية وتغطي جوانب مختلفة من هذا المجال، مثل:
- تطوير المواد وآليات التحكم للروبوتات الدقيقة [1، 7، 35]
- التطبيقات الطبية للروبوتات الدقيقة في مختلف الأعضاء والأنظمة الجسمية [3، 5، 45]
- تقنيات التصوير لتتبع الروبوتات الدقيقة داخل الجسم [11، 12، 21]
- التحديات والتوجهات المستقبلية في أبحاث الروبوتات الدقيقة [30، 48، 65]
إذا كنت مهتمًا بجانب محدد من الروبوتات الدقيقة لتوصيل الأدوية المستهدفة، يمكنك الرجوع إلى المراجع المقابلة في القائمة. على سبيل المثال، إذا كنت مهتمًا باستخدام المجالات المغناطيسية للتحكم في الروبوتات الدقيقة، يمكنك الاطلاع على المراجع [6، 15، 35].
إليك تفصيلاً لبعض المراجع الرئيسية المضمنة:
- المراجعات: تقدم المراجع [5، 8، 31] نظرة عامة شاملة على الروبوتات الدقيقة لتوصيل الأدوية، وتناقش تصميمها وطرق تشغيلها وتطبيقاتها المحتملة.
- الروبوتات الدقيقة المغناطيسية: هذا نهج شائع بسبب سهولة التحكم فيها باستخدام المجالات المغناطيسية الخارجية. راجع المراجع [6، 16، 35] لمزيد من التفاصيل.
- الروبوتات الدقيقة الهجينة الحيوية: هذه الروبوتات تجمع بين المكونات البيولوجية والمواد الاصطناعية، مما يوفر التوافق البيولوجي وقدرات التوصيل المستهدف. المرجع [14] هو مثال.
- التصوير والملاحة: تتبع الروبوتات الدقيقة في الوقت الفعلي داخل الجسم أمر بالغ الأهمية. تناقش المراجع [11، 21، 25] مختلف تقنيات التصوير المستخدمة لهذا الغرض.
آمل أن يساعدك هذا!
المراجع والملاحظات هنا : https://areaangel.blogspot.com/2024/04/blog-post_9.html










 رد مع اقتباس
رد مع اقتباس